REVIEW
KIMIA DASAR
PERTEMUAN
KELIMA

NAMA
: LUFITA
NIM
: A1C217021
DOSEN
PENGAMPU : Dr. YUSNELTI, M.Si
PRODI PENDIDIKAN MATEMATIKA
JURUSAN
MATEMATIKA DAN IPA
FAKULTAS
KEGURUAN DAN ILMU PENDIDIKAN
UNIVERSITAS
JAMBI
2017
BAB 1
PENDAHULUAN
1. Latar Belakang
Sejalan dengan perkembangan ilmu pengetahuan
dan teknologi, manusia tidak dapat terlepas dari berbagai bentuk masalah dalam
kehidupan, olehnya para ilmuan selalu mengkaji persoalan yang terjadi baik
dalam lingkungan maupun alam secara keseluruhan. Dengan hal tersebut sejarah
perkembangan yang diangkat lewat latar belakang ini adalah sejarah perkembangan
sistem periodik unsur mulai dari pengelompokan yang secara modern. Sistem
periodik merupakan suatu cara untukn mengelompokkan unsur-unsur berdasarkan
sifatnya. Pengelompokkan unsur mengalami sejarah perkembangan, sifat logam, non
logam, hukum-hukum, golongan, periode dari sifat-sifat unsur dalam sistem
periodik modern.
Sampai saat ini sudah ditentukan 115 macam
unsur dengan sifat-sifat yang khas pada setiap unsur. Puncak dari usaha-usaha
para ahli tersebut adalah terciptanya suatu daftar yang disebut sistem periodik
unsur. Sistem periodik unsur ini mengandung banyak informasi mengenai
sifat-sifat unsur sehingga dapat membantu kita dalam mempelajari dan mengenali
unsur-unsur yang kini jumlahnya 115 macam.
2. Tujuan
2.1 mengetahui susunan berkala dan beberapa sifat unsur
2.2 mengetahui beberapa sifat unsur
2.3 mengetahui susunan berkala tahap pertama
2.4 mengetahui pandangan terbaru tentang atom
2.5 menegtahui nomor atom dan tabel periodik yang baru
2.6 menegtahui reaksi logam dan non logam : pembentukan senyawa ion
2.7 mengetahui rekasi antara unsur nonlogam : pembentukan senyawa molekuler
2.8 mengetahui beberapa sifat senyawa ionik dan senyawa molekuler
2.9 mengetahui reaksi oksidasi dan reduksi
2.10 mengetahui cara memberi nama senyawa kimia
BAB 2
PEMBAHASAN
2.1
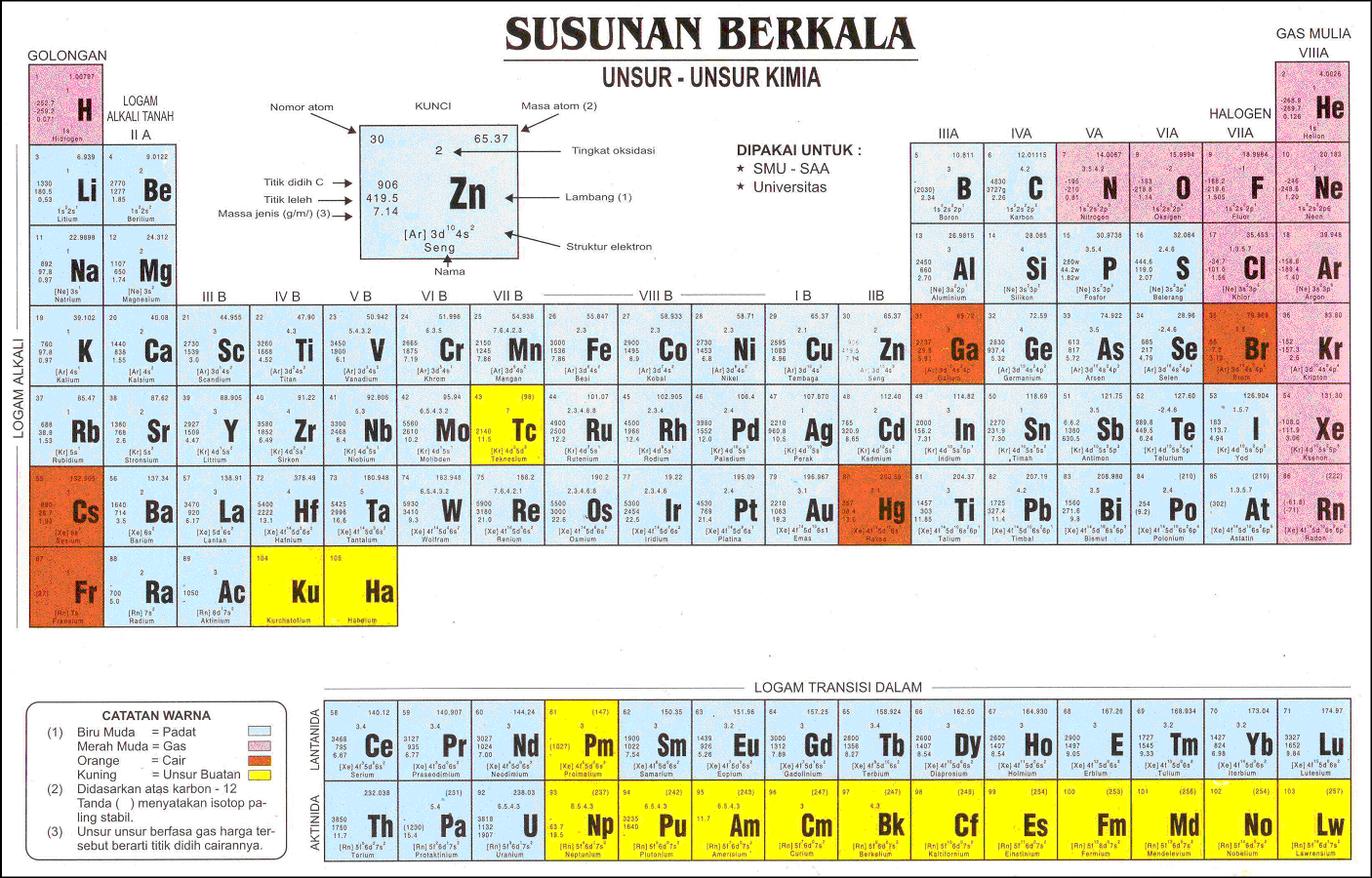
SUSUNAN BERKALA DAN BEBERAPA SIFAT UNSUR
Susunan Berkala disebut juga sebagai sistem periodik unsur. Dengan ilmu
kimia kita dapat mempelajari segala sesuatu tentang unsur-unsur dan interaksi
antara suatu unsur dengan unsur yang lainnya, sehingga dapat terjadi suatu
perubahan kimia (reaksi kimia persenyawaan dan lain-lain).
Seperti
kita ketahui, telah dikenal lebih dari 100 unsur terdapat di alam dan
masing-masing unsur memiliki sifat-sifat yang berbeda. Oleh karena itu untuk
mempelajari kelakukan setiap unsur, perlu diadakan klasifikasi unsur-unsur
dalam golongan-golongan yang didasarkan atas persamaan sifat-sifatnya.
Unsur-unsur yang memiliki sifat-sifat yang mirip dimasukan ke dalam satu
golongan, sehingga dapat dipelajari dengan lebih mudah dan lebih sistimatis,
sekaligus dapat melihat hubungan antara satu hal dengan hal lainnya. Secara
singkat, guna susunan berkala adalah untuk meramalkan dan mengetahui sifat
unsur, sehingga kita dapat meramalkaan dan mengetahui berbagai gejala/kejadian
di alam.
Konfigurasi
elektron 20 unsur pertama dalam Sistem Periodik
1.
Periode
Periode ditempatkan pada lajur horizontal dalam sistem periodik modern.
Periode suatu unsur menunjukan suatu nomor kulit yang sudah terisi elektron (n
terbesar) berdasarkan konfigurasi elektron. Konfigurasi elektron adalah
persebaran elektron dalam kulit-kulit atomnya.
Dalam
sistem periodik modern terdapat 7 periode, yaitu :
1. Periode 1 (periode sangat pendek) berisi 2 unsur, yaitu H dan He.
2. Periode 2 (periode pendek) berisi 8 unsur yaitu, Li, Be, B, C, N, O, F, Ne.
3. Periode 3 (periode pendek) berisi 8 unsur, yaitu Na, Mg, Al, Si, P, S, Cl,
Ar.
4. Periode 4 (periode panjang) berisi 18 unsur, yaitu K, Ca, Sc, Ti, V, Cr,
Mn, Fe, Co, Ni, Cu, Zn, Ga, Ge, As, Se, Br, Kr.
5. Periode 5 (periode panjang) berisi 18 unsur, yaitu Rb, Sr, Y, Zr, Nb, Mo,
Tc, Ru, Rh, Pd, Ag, Cd, In, Sn, Sb, Te, I, Xe.
6. Periode 6 (periode sangat panjang)berisi 32 unsur yaitu, 18 unsur seperti
pada periode 4 atau ke-5, yaitu Cs, Ba, La, Hf, Ta, W, Re, Os, Ir, Pt, Au, Hg,
Tl, Pb, Bi, Po, At, Rn, dan 14 unsur lagi merupakan deret lantanida, yaitu Ce,
Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu;
7. Periode 7 (periode sangat panjang) berisi 28 unsur, yaitu Fr, Ra, Ac, Rf,
Db, Sg, Bh, Hs,Mt, Uun, Uuu, Uub, Uut, Uuq, Uup, Uuh, Uus Uuobelum lengkap
karena maksimum 32 unsur. Pada periode ini terdapat deret aktinida yaitu Th,
Pa, U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr.
2.
Golongan
Golongan adalah lajur tegak pada tabel periodik unsur. Unsur-unsur yang ada
dalam satu lajur tegak adalah unsur-unsur segolongan, terdapat delapan golongan
utama dan delapan golongan transisi.
a. Golongan
utama
Golongan
utama tersebut adalah :
1. Golongan I A disebut golongan alkali (kecuali H) terdiri dari unsur-unsur :
H, Li, Na, K, Rb, Cs, Fr .
2. Golongan II A disebut golongan alkali tanah yang terdiri dari unsur-unsur :
Be, Mg, Ca, Sr, Ba, Ra.
3. Golongan III A disebut golongan baron aluminium yang terdiri dari
unsur-unsur:
B, Al, Ga, In, Ti, Uut.
4. Golongan IV A disebut golongan karbon-silicon yang terdiri dari unsur-unsur
:
C, Si, Ge, Sn, Pb, Uuq.
5. Golongan V A disebut golongan nitrogen-fosforus yang terdiri dari
unsur-unsur:
N, P, As, Sb, Bi, Uup.
6. Golongan VI A disebut golongan oksigen-belerang yang terdiri dari
unsur-unsur:
O, S, Se, Te, Po, Uuh.
7. Golongan VII A disebut golongan halogen yang terdiri dari unsur-unsur :
F, Cl, Br, I, At.
8. Golongan VIII A disebut golongan gas mulia yang terdiri dari unsur-unsur :
He, Ne, Ar, Kr, Xe, Rn.
b. Golongan
transisi
Golongan
transisi tersebut adalah :
a. Golongan I B terdiri dari unsur-unsur Cu, Ag, Au, Rg.
b. Golongan II B terdiri dari unsur-unsur Zn, Cd, Hg, Uub.
c. Golongan III B terdiri dari unsur-unsur Se,Y, La, Ac.
d. Golongan IV B terdiri dari unsur-unsur Ti, Zr, Hf, Rf.
e. Golongan V B terdiri dari unsur-unsur V, Nb, Ta, Db.
f.
Golongan VI B terdiri dari unsur-unsur
Cr, Mo, W, Sg.
g. Golongan VI B terdiri dari unsur-unsurMn, Te, Re,Bh.
h. Golongan VIII B terdiri dari unsur-unsur Fe, Ru, Os, Hs, Co, Rh, Ir, Mt,
Ni, Pd, Pt, Ds.
Pada
periode 6 dan 7 terdapat masing-masing 14 unsur yang disebut unsur-unsur
transisi dalam, yaitu unsur-unsur antanida dan aktinida. Unsur-unsur transisi
dalam semua termasuk golongan IIIB. Unsur-unsur lantanida pada periode 6
golongan IIIB, dan unsur-unsur aktinida pada periode 7 golongan IIIB.
Penempatan unsur-unsur tersebut di bagian bawah tabel periodik adalah untuk
alasan teknis, sehingga daftr tidak terlalu panjang.
2.2
BEBERAPA SIFAT UNSUR
1.
Jari-jari Atom
Jari-jari atom adalah jarak dari inti atom ke kulit terluar. Besarnya
jari-jari atom dipengaruhi oleh jumlah kulit elektron dan muatan inti atom.
Dalam
suatu golongan, jari-jari atom semakin ke atas cenderung semakin kecil. Hal ini
terjadi karena semakin ke atas, kulit elektron semakin kecil.
Dalam
suatu periode, semakin ke kanan jari-jari atom cenderung semakin kecil. Hal ini
terjadi karena semakin ke kanan jumlah proton dan jumlah elektron semakin
banyak, sedangkan jumlah kulit terluar yang terisi elektron tetap sama sehingga
tarikan inti terhadap elektron terluar semakin kuat.
2.
Jari-jari Ion
Ion mempunyai jari-jari yang berbeda secara nyata (signifikan) jika
dibandingkan dengan jari-jari atom netralnya. Ion bermuatan positif (kation)
mempunyai jari-jari yang lebih kecil, sedangkan ion bermuatan negatif (anion)
mempunyai jari-jari yang lebih besar jika dibandingkan dengan jari-jari atom
netralnya.
3.
Energi Ionisasi
Energi ionisasi adalah besarnya energi yang diperlukan oleh suatu atom/ion
untuk melepaskan sebuah elektron yang terikat paling lemah (elektron teluar).
Energi
ionisasi merupakan energi yang digunakan untuk melawan gaya tarik inti terhadap
elektron terluarnya, jadi semakin jauh dari inti maka semakin kecil energi
ionisasinya dan semakin mudah elektron itu dilepaskan.
Dalam
suatu periode semakin banyak elektron dan proton gaya tarik menarik elektron
terluar dengan inti semakin besar (jari-jari kecil). Akibatnya, elektron sukar
lepas sehingga energi untuk melepas elektron semakin besar. Hal ini berarti
energi ionisasi besar. Jika jumlah elektronnya sedikit, gaya tarik menarik
elektron dengan inti lebih kecil (jari-jarinya semakain besar). Akibatnya,
energi untuk melepaskan elektron terluar relatif lebih kecil berarti energi
ionisasi kecil.
·
Unsur-unsur yang segolongan : energi
ionisasi makin ke bawah makin kecil, karena elektron terluar makin jauh dari
inti (gaya tarik inti makin lemah), sehingga elektron terluar makin mudah di
lepaskan.
·
Unsur-unsur yan seperiode : energi
ionisai pada umumnya makin ke kanan makin besar, karena makin ke kanan gaya
tarik inti makin kuat.
Kekecualian
:
Unsur-unsur
golongan II A memiliki energi ionisasi yang lebih besar dari pada golongan III
A, dan energi ionisasi golongan V A lebih besar dari pada golongan VI A.
4.
Afinitas Elektron
Afinitas Elektron adalah besarnya energi yang dibebaskan oleh suatu atom
untuk menerina sebuah elektron.
Jadi,
besaran afinitas elektron merupakan besaran yang dapat digunakan untuk mudah
tidaknya atom untuk menarik elektron. Semakin besar afinitas elektron yang
dimiliki atom itu menunjukan bahwa atom itu mudah nenarik elektron dari luar
dan membentuk ion negatif(anion). Jika ion negatif yang terbentuk bersifat
stabil, maka proses penyerapan elektron itu disertai pelepasan energi dan
afinitas elektronnya dinyatakan dengan tanda negatif. Akan tetapi jika ion
negatif yang terbentuk tidak stabil, maka proses penyerapan elektron akan
membutuhkan energi dan afinitas elektronnya dinyatakan dengan tanda positif.
Jadi, unsur yang mempunyai afinitas elektron bertanda negatif mempunyai
kecenderungan lebih besar menyerap elektron daripada unsur yang afinitas
elektronnya bertanda positif. Makin negatif nilai afinitas elektron berarti
makin besar kecenderungan menyerap elektron.
Dalam
satu periode dari kiri ke kanan, jari-jari semakin kecil dan gaya tarik inti
terhadap elektron semakin besar, maka atom semakin mudah menarik elektron dari
luar sehingga afinitas elektron semakin besar.
Pada
satu golongan dari atas ke bawah, jari-jari atom makin besar, sehingga gaya
tarik inti terhadap elektron makin kecil, maka atom semakin sulit menarik
elektron dari luar, sehingga afinitas elektron semakin kecil.
Dalam
satu periode, dari kiri ke kanan afinitas elektron bertambah.
Dalam satu
golongan, dari atas ke bawah afinitas elektron berkurang.
5.
Keelektronegatifan
Keelektronegatifan adalah kemampuan suatu atom untuk menarik elektron dari
atom lain. Faktor yang mempengaruhi keelektronegatifan adalah gaya tarik dari
inti terhadap elektron dan jari-jari atom. Harga keelektronegatifan bersifat
relatif (berupa perbandingan suatu atom yag lain).
·
Unsur-unsur yang segolongan :
keelktronegatifan makin ke bawah makin kecil, karena gaya taik-menarik inti
makin lemah. Unsur-unsur bagian bawah dalam sistem periodik cenderung
melepaskan elektron.
·
Unsur-unsur yang seperiode :
keelektronegatifan makin ke kanan makin besar. Keelektronegatifan terbesar pada
setiap periode dimiliki oleh golongan VII A (unsur-unsur halogen). Harga
keelektronegatifan terbesar terdapat pada flour (F) yakni 4,0, dan harga
terkecil terdapat pada fransium (Fr) yakni 0,7.
Harga
keelektronegatifan penting untuk menentukan bilangan oksidasi (biloks) unsur
dalam sutu senyawa. Jika harga keelektronegatifan besar, berarti unsur yang
bersangkutan cenderung menerim elektron dan membentuk bilangan oksidasi
negatif. Jika harga keelektronegatifan kecil, unsur cenderung melepaskan
elektron dan membentuk bilangan oksidasi positif. Jumlah atom yang diikat
bergantung pada elektron valensinya.
6.
Sifat Logam dan Non Logam
Sifat-sifat unsur logam yang spesifik, antara lain : mengkilap,
menghantarkan panas dan listrik, dapat ditempa menjadi lempengan tipis, serta
dapat ditentangkan menjadi kawat/kabel panjang. Sifat-sifat logam tersebut diatas
yang membedakan dengan unsur-unsur bukan logam. Sifat-sifat logam, dalam sistem
periodik makin kebawah makin bertambah, dan makin ke kanan makin berkurang.
Batas
unsur-unsur logam yang terletak di sebelah kiri dengan batas unsur-unsur bukan
logam di sebelah kanan pada sistem periodik sering digambarkan dengan tangga
diagonal bergaris tebal. Unsur-unsur yang berada pada batas antara logam dengan
bukan logam menunjukkan sifat ganda.
Contoh :
·
Berilium dan Aluminium adalah logam yang
memiliki beberapa sifat bukan logam. Hal ini disebut unsur-unsur amfoter.
·
Baron dan Silikon adalah unsur bukan
logam yang memiliki beberapa sifat logam. Hal
ini
disebut unsur-unsur metalloid.
7.
Kereaktifan
Reaktif artinya mudah bereaksi. Unsur-unsur logam pada sistem periodik,
makin ke bawah makin reaktif, karena makin mudah melepaskan elektron.
Unsur-unsur bukan logam pada sistem periodik, makin ke bawah makin kurang
reaktif, karena makin sukar menangkap elektron.
Kereaktifan
suatu unsur bergantung pada kecenderungannya melepas atau menarik elektron.
Jadi, unsur logam yang paling reatif adalah golongan VIIA (halogen). Dari kiri
ke kanan dalam satu periode, mula-mula kereaktifan menurun kemudian bertambah
hingga golongan VIIA. Golongan VIIA tidak reaktif.
2.3 SUSUNAN BERKALA YANG PERTAMA
Pada permulaannya percobaan-percobaan yang dilakukan untuk
mengklasifikasikan unsur hasilnya sangat terbatas dan tidak sampai pada tahun
1869, pelopor daftar periodik yang modern menemukan cara untuk mengatasinya.
Penemuan ini merupakan hasil kerja dua ahli kimia, Dmitri Mendeleev dari Rusia
dan Julius Lothar Meyer dari Jerman. Mereka bekerja secara terpisah, tetapi
menghasilkan daftar periodik yang sama pada waktu yang hampir bersamaan.
Mendeleev mempresentasikan hasil kerjanya di depan Persatuan Ahli Kimia Rusia
(Russian Chemical Society) pada permulaan tahun 1869, tetapi daftar periodik
Meyer belum muncul sampai bulan December tahun itu. Dalarn-hal ini Mendeleev
lebih beruntung karena telah memperagakan lebih dahulu penemuannya, sehingga dia
Iebih dikenal sebagai penemu daftar periodik.
Mendeleev adalah seorang guru kimia, dimana ketika dia mempersiapkan buku
penuntun (text book) untuk muridnya, dia menemukan bahwa jika unsur disusun
menurut massa atom yang menaik, unsur dengan sifat-sifat yang sama akan
dijumpai jarak (interval) secara periodik (periodic interval). sebagai contoh,
diambilnya unsur litium (Li), natrium (Na), kalium (K), dan rubidium (Rb).
Setiap unsur membentuk senyawa yang larut dalam air jika direaksikan dengan
khlor dengan rumus urnum MCI, dimana M adalah Li, Na, K dan seterusnya. Meskipun
hal ini suatu kenyataan yang menarik, yang paling penting adalah bahwa jika
kita teliti unsur setelah Li, Na, K dan Rb dalam daftar (Be, Mg, Ca dan Sr,
misalnya), unsur-unsur ini juga termasuk grup unsur yang sama. Misalnva unsur
ini membentuk senyawa’BeCl2, MgCl2, CaCl2 dan
SrCl2,. Mendeleev menemukan fakta (phenomena) seperti ini
terjadi berulang-ulang dalam daftar unsurnya dan dia sadar bahwa daftar ini
dapat dibaginya menjadi beberapa seri barisan (row). Jika satu deratan unsur
terletak di atas deretan yang lain, maka deretan unsur itu mempunyai sifat
yang sama dalam kolom vertikal. Hasilnya adalah merupakan susunan berkala yang
pertama.
Ketika
Mendeleev menyusun hal ini, belum semua unsur ditemukan. Dia menyadari hal ini,
karena untuk selalu memperoleh unsur yang sama dalam satu kolom atau grup, dia selalu terpaksa
mengosongkan tempat dalam daftarnya. Hal ini juga diperlakukannya untuk
membalik susunan massa atom, misalnya tellurium (Te) dan iodium (I), dimana
massa atomnya dalam tahun 1869 diduga adalah 128 dan 127 u, Mendeleev
menempatkan unsur dalam susunan yang terbalik (menurut massa atom), karena
sifat-sifatnya menunjukkan tellurium masuk dalam kelompok (grup) VI dan iodium
dalam kelompok VII (Golongan ditulis dengan angka Romawi untuk memudahkan
penandaan).
Salah satu keuntungan daftar Mendeleev
adalah memungkinkan membuat perkiraaan sifat-sifat unsur yang masih kosong
dalam daftar. Sebab unsur yang ada dalam setiap kolom tertentu mempunyai sifat
yang sama. Sebagai contoh germanium yang terletak di bawah silikon dan di atas
timah putih dalam Kelompok IV, belum ditemukan ketika Mendeleev menyusun daftar
ini. Oleh karena itu pada pita yang dibuatnya ditemukan kolom yang kosong.
Berdasarkan letak elemen itu, Mendeleev dapat menduga sifat unsur ini yang
disebutnya "eka-silikon", yang hares terletak antara silikon dan
timah putih.
Jika kita lihat daftar periodik yang
terbaru, kita jumpai unsur-unsur yang tidak ada dalam daftar Mendeleev. Kolom
ini sangat penting dengan judul Gas Mulia ("Noble Gases"). Unsur ini
sangat tidak reaktif, dalam bentuk gas yang tidak berwarna dan tidak berbau,
dalam jumlah yang sangat sedikit diatmosfir. Karena unsur ini tidak dikenal
senyawanya, maka para ilmuwan dimana Mendeleev tidak tahu adanya unsur ini.
Setelah unsur ini ditemukan, diketahui bahwa massa atom argon. agak lebih besar
dari kalium (K). Kenyataannya, kalium jelas masuk dalam unsur Kelompok I dan
argon jelas masuk dalam kolompok gas mulia. Kembali lagi seperti terjadi pada
Te dan I, sangat penting menempatkan sepasang unsur dalam daftar menurut massa
atom yang terbalik (reverse).
Kebutuhan untuk memindahkan daftar massa
atom dari kedua pasang unsur ini, menyebabkan para ilmuwan sadar akhimya, bahwa
massa atom tidak menentukan sekali dimana elemen ditempatkan dalam daftar
berkala. Dasar yang sebetulnya menentukan daftar periodik dapat terletak dimana
saja, seperti yang akan kita bicarakan dalam uraian
2.4 PANDANGAN TERBARU TENTANG ATOM
Permasalahan yang dijumpai jika elemen
disusun dalam daftar berkala Mendeleyev menurut aturan massa-atom akan hilang,
jika unsur-unsur ini disusun menurut nomor atomnya. Untuk memahami nomor
atom, maka kita harus mula-mula melihat struktur bagian dalam dari
atom. Pandangan Dalton mengenai atom sebagai bagian yang paling kecil
(partikel) yang tidak dapat dibagi, kita ketahui sekarang bahwa hal ini tidak
benar. Eksperimen-eksperimen yang telah dimulai sejak alkhir abad ke sembilan
betas dan dilanjutkan sampai sekarang memperlihatkan bahwa atom itu sendiri
terdiri dari partikel-partikel subatom. Banyak partikel ini
yang telah diketahui, tetapi suatu yang prinsip, yang sangat penting kita
ketahui adalah proton, neutron, dan elektron.
Proton dan elektron merupakan partikel
yang bermuatan listrik. Proton dan elektron ini membawa muatan yang berbeda,
dimana proton mempunyai muatan yang ditetapkan dengan tanda positif (+) dan
elektron mempunyai muatan yang ditetapkan dengan tanda negatif (-). Suatu
hal yang sangat penting dipahami mengenai muatan listrik ini adalah muatan yang
berlawanan akan sating tarik menarik dan muatan yang sama saling tolak menolak.
Jadi, proton menarik elektron, tetapi proton menolak proton dan elektron
menolak elektron. Neutron, sesuai dengan namanya, tidak bermuatan, dengan
demikian muatan listriknya netral.
Dalam SI, muatan listrik ditetapkan
dalam coulomb (simbolnya Q). Satu coulomb adalah jumlah muatan
listrik yang melalui titik-titik yang telah ditentukan dalam suatu kawat jika
arus listrik sebesar 1 Amper melaluinya selama 1 detik. Dalam istilah yang
lebih umum, jika bola lampu 100 watt bersinar, maka dibutuhkan waktu 1,2 detik
larnanya muatan listrik melalui kawat bola lampu itu agar diperoleh muatan 1
coulomb. Jumlah muatan ini cukup besar, tetapi jumlah muatan yang dibawa oleh
satu elektron sangat kecil, yaitu sebesar 1,60 x 10-19 C.
Karena muatan elektron adalah negatif, maka muatannya adalah -1,60 •x 10-19 C.
Proton juga mempunyai muatan yang sama dengan elektron, tetapi dengan muatan
yang berlawanan, jadi muatan proton adalah +1,60 x 10-19 C.
Jika kita menghitung muatan listrik
partikel, selalu dikalikan dengan 1,60 x 10-19 C,
dengan demikian lebih sesuai untuk menyederhanakan satu unit muatan listrik
sama dengan jumlah ini. Dalam Skala ini, suatu elektron mempunyai satu unit
muatan negatif (disebut muatannya 1-) dan suatu proton mempunyai satu unit
muatan positif (disebut muatannya 1 +).
Partikel subatom ini juga mempunyai
sifat lain yang penting yaitu massanya. Proton dan neutron adalah partikel yang
relatif berat yang massanya kira-kira satu unit massa atom (1u). Sebaliknya
elektron adalah partikel yang ringan dengan massa hanya kira-kira 1/1836 dari
massa proton.
2.5 NOMOR ATOM DAN TABEL
PERIODIK YANG BARU
Jika unsur disusun dalam susunan berkala
menurut nomor atom, semua hal yang masih diragukan yang dijumpai dalam tabel
Mendeleev menjadi hilang. Tellurium dan indium, argon dan kalium tersusun
dengan sendirinya ke tempat dimana unsur ini seharusnya. Jadi, terbukti nomor
atom suatu unsur--jumlah proton dalam inti atom tersebut menentukan dimana
unsur tersebut ditempatkan dalam tabel dan setiap unsur dengan sifat yang sama
dijumpai dalam kelompok yang sama, dan nomor atom elemen tersebut pasti
menentukan macam-macam sifat kimia dan fisika unsur tersebut. Untuk sekarang,
marilah kita perhatikan susunan berkala baru telah disusun, dimana kita dapat
mengetahui cara menggunakannya untuk menghubungkan sifat kimia dan sifat fisika
suatu unsur.
Susunan berkala yang sekarang digunakan
dapat dilihat pada Gambar . Angka yang dicetak di atas simbol kimia adalah
nomor atom dan yang di bawah adalah massa atom. Sama seperti tabel Mendeleev,
tabel ini terdiri dari sejumlah kolom sejajar (row) yang disebut berkala/periodik yang ditandai
dengan angka biasa (Arab) dan kolom vertikal yang disebut kelompok/golongan (group), dimana
setiap golongan mengandung satu keluarga unsur Golongan ini juga
ditandai dengan angka. Sistem penomoran yang selama ini dipakai di Amerika
Serikat hampir sama dengan sistim Mendeleev dan setiap golongan/grup
menggunakan angka Romawi dan huruf A atau B. Hal ini dapat dilihat pada bagian
atas setiap kelompok/grup. Baru-baru ini, International Union of Pure and
Applied Chemistry (IUPAC) menyetujui suatu sistim alternatif dimana
golongan/grup diberi nomor dari kiri ke kanan dimulai dari 1 sampai 18. Angka
ini diletakkan di bawah penandaan Romawi. Sistim baru ini telah menimbulkan
perdebatan yang hebat, banyak ahli kimia pengajar ilmu kimia menentangnya.
Karena ketentuan ini masih diperdebatkan, maka kita akan menggunakan penomoran
menurut angka Romawi dan golongan/grup A dan B.
Golongan yang dikiri tanda dengan huruf
A (golongan I A sampai VII A) dan golongan 0 menunjukkan kebersamaan (kolektif)
sebagai elemen representatif (representative
element). Label dengan huruf B (golongan I B sampai VII B) ditambah golongan
VIII (sebetulnya terdiri dari tiga kolom yang pendek yang terletak ditengah
tabel) disebut elemen transisi (transition
element). Alasan penandaan golongan A dan B adalah karena ada beberapa kesamaan
sifat antara unsur kelompok A dan elemen kelompok B, meskipun kesamaan sifat
tersebut kadang-kadang sedikit.
Akhirnya ada dua baris unsur yang
diletakkan tepat di bawah bagian utama tabel. Unsur ini dikenal dengan
nama unsur transisi bagian dalam (inner transition
element), sebetulnya merupakan bagian dari bagan yang ada dalam tabel seperti
terlihat dalam Gambar. Unsur ini biasanya diletakkan di bawah bagan yang telah
disiapkan (conserve space), dengan demikian tabel dapat dicetak lebih menarik,
seingga huruf-huruf tidak terlalu kecil untuk dapat dibaca. Perhatikan Gambar,
terlihat baris pertama unsur transisi bagian dalam terletak setelah unsur
lanthanum (La) dan baris kedua setelah unsur actinium (Ac). Karena unsur ini
terletak mengik-un baris ini, maka baris pertama (unsur 58 sampai 71)
disebut lantanida (lanthanides) dan baris kedua (90 sampai
103)disebut aktinida (actinides). Sering juga disebut,
lantanida sebagai unsur yang jarang dijumpai di bumf (rare
earth element), karena sangat sedikit ditemukan dalam kerak bumf.
Sebagian unsur mempunyai nama yang
khusus, demikian juga jum lah kelompoknya. sebagai contoh, unsur Golongan I A
(diluar hidrogen) dikenal dengan nama logam alkali dan unsur
Golongan II A logam alkali tanah. Unsur golongan VIIA
adalah halogen, nama ini diambil dari bahasa Yunani, yang
berarti "pembuat garam-salt-former". Akhirnya unsur Golongan 0
(angka nol) disebut gas mulia (juga kadang-kadang disebut
gas invert) karena elemen ini sangat sukar bereaksi.
2.6 REAKSI LOGAM DENGAN NONLOGAM : PEMBENTUKAN SENYAWA
ION
Senyawa ionik adalah senyawa kimia yang
terbentuk oleh muatan listrik yang oleh masing-masing ion atom penyusunnya.
Biasanya senyawa ionik terdiri dari unsur logam bermuatan positif dan non logam
bermuatan negatif dan berbentuk struktur kristal. Garam dapur NaCl adalah
senyawa ionik paling umum yang terdiri dari atom natrium (logam) bermuatan
positif dan atom klor (non logam) bermuatan negatif. Beberapa karakteristik
senyawa ionik antara lain memiliki titik didih dan titik leleh tinggi serta
memiliki struktur berbentuk kristal.
Penamaan
senyawa ionik dilakukan dengan pertama menyebutkan kation (ion bermuatan
positif) dan diikuti dengan penyebutan anion (ion bermuatan negatif). Contoh
nama – nama senyawa dengan ikatan ionik diantaranya adalah natrium klorida,
kalium iodida, perak nitrat, dan merkuri klorida. Jumlah atom kation positif
dan anion negatif tidak termasuk dalam struktur penamaan. Sebagai contoh, perak
nitrar dengan rumus kimia AgNO3 tidak memerlukan bentuk jamak untuk
kelompok nitrat.
Contoh : 2Na(s) + Cl2(g) ―›
2NaCl (s)
Mg(s) + Cl 2(g) ―›
MgCl 2(s)
2.7 REAKSI DIANTARA UNSUR NONLOGAM : PEMBENTUKAN
SENYAWA MOLEKULER
Senyawa
molekuler: mereka biasanya ada dalam keadaan cair atau gas pada suhu dan
tekanan standar. Hal ini karena kekuatan yang lemah tarik – menarik antara atom
membentuk ikatan kovalen.
Senyawa molekul untuk menjadi lebih
singkat disebut molekul. Sebagian besar senyawa molekul yang ada mengandung
banyak atom seperti gula pasir, sukrosa, yang secra kimia ditulis sebagai C12
H22 O11. Ini berarti bahwa ia memiliki 12 atom karbon, 22
atom hidrogen, 22 atom hidrogen, dan 11 atom oksigen.
Dalam senyawa molekul, daya tarik atom
disebut ikatan kovalen. Senyawa molekul sebenarnya sama dengan senyawa kovalen,
hal-hal yang sama dengan nama berbeda. Senyawa molekul biasanya memiliki sifat
konduktivitas listrik sedikit atau tidak ada. Jenis senyawa yang sering
terbentuk antara dua non logam.
Contoh : C(S) + O2(g) ―› CO2(g)
C(s) + O2(g) ―› 2CO(g)
Karbonmonoksida sendiri mampu berekasi dengan okosigen
membentuk CO2
2CO(g) + O2(g) ―› 2CO2(g)
2.8 BEBERAPA SIFAT SENYAWA IONIK DAN SENYAWA MOLEKULER
Senyawa ionik : senyawa ionik biasanya dalam keadaan
padat pada suhu dan tekanan standar (STP). Hal ini dikarenakan daya tarik yang
kuat antara ion bermuatan positif dan mereka bermuatan negatif. Mereka
membentuk struktur kristal yang disebut kisi kristal.
Senyawa molekul : mereka biasanya ada dalam keadaan
cair atau gas pada suhu dan tekanan standar. Hal ini karena kekuatan yang lemah
tarik – menarik antara atom membentuk ikatan kovalen.
Sifat
Senyawa Ionik adalah sebagai berikut :
1.
Titik Lebur Tinggi
Ikatan ionik kuat dikarenakan tarikan antara Anion dan Kationnya kuat / besar
oleh karena itu,ikatan ionik sulit diputus,sehingga memerlukan energi yang besar untuk memutus ikatan ionik,oleh karena itu titik leburnya tinggi.
Ikatan ionik kuat dikarenakan tarikan antara Anion dan Kationnya kuat / besar
oleh karena itu,ikatan ionik sulit diputus,sehingga memerlukan energi yang besar untuk memutus ikatan ionik,oleh karena itu titik leburnya tinggi.
2.
Kemampuan menghantarkan listrik
a) Fase Padat
a) Fase Padat
e
—> +-+-+-
-+-+-+
karena susunan antara proton dan elektron rapat,sehingga elektron dari luar susah mengalir,oleh karena itu,senyawa ionik pada fase padat tidak dapat menghantarkan listrik.
-+-+-+
karena susunan antara proton dan elektron rapat,sehingga elektron dari luar susah mengalir,oleh karena itu,senyawa ionik pada fase padat tidak dapat menghantarkan listrik.
b)
Fase Cair
+ –
– +
Karena susunan antara proton dan elektronnya renggang,maka elektron mudah mengalir,sehingga senyawa ionik pada fase cair dapat menghantarkan listrik.
+ –
– +
Karena susunan antara proton dan elektronnya renggang,maka elektron mudah mengalir,sehingga senyawa ionik pada fase cair dapat menghantarkan listrik.
3.
Keras tapi Rapuh
Kation
dan Anion penyusun senyawa ionik pada mulanya saling tarik menarik,namun
setelah ditempa,terjadi pergeseran ion-ion penyusun senyawa ionik,sehingga
menimbulkan tolakan antara Kation dengan Kation atau Anion dengan Anion,setelah
itu padatan akan pecah.
4.
Larut dalam pelarut air
NaCl
—–> Na+ + Cl-
“dalam
air,senyawa ionik akan terion menjadi ionnya (+ dan -)
Catatan
:
“Gol IVA cenderung menangkap elektron,sehingga energi untuk menangkap 4 elektron lebih kecil”
“Gol IVA cenderung menangkap elektron,sehingga energi untuk menangkap 4 elektron lebih kecil”
Perbedaan
antara senyawa ionik dan senyawa molekul
Ø Entalpi
fusi (energi panas yang diserap bila padat mencair) dan entalpi penguapan
(energi panas yang diserap ketika cairan mendidih) lebih tinggi dalam senyawa
ion.
Ø Senyawa
molekuler lebih mudah terbakar di bandingkan senyawa ion.
Ø Senyawa
molekuler lebih lembut dan lebih fleksibel dibandingkan dengan senyawa ion.
Ø Senyawa
ionik memiliki titik leleh dan titik didih lebih tinggi dari senyawa molekul.
Ø Senyawa
ionik bermuatan ion, sedangkan senyawa molekul terdiri dari molekul.
Ø Suatu
senyawa ionik dibentuk oleh reaksi dari logam dengan non logam, sedangkan
senyawa molekul biasanya dibentuk oleh reaksi dari dua atau lebih non logam.
Ø Dalam
senyawa ion, ion-ion yang diadakan bersama-sama karena daya tarik listrik,
sedangkah dalam senyawa molekul atom yang diselenggarakan bersama oleh daya
tarik antara atom karena elektron bersama.
Ø Senyawa
molekul tidak dapat menghantarkan listrik di setiap keadaan, sedangkan senyawa
ion, jika dilarutkan dalam larutan berair dapat bertindak sebagai konduktor
listrik yang baik.
Ø Senyawa
ionik lebih reaktif daripada senyawa molekuler.
2.9 REAKSI
OKSIDASI REDUKSI
Reaksi
redoks adalah reaksi kimia yang disertai perubahan bilangan okdidasi atau
reaksi yang didalamnya terdapat serah terima elektron antar zat
Pengertian
oksidasi dan reduksi dapat ditinjau berdasarkan 3 landasan teori, yaitu :
1. Reaksi
Pengikatan dan pelepasan unsur oksigen
Reaksi
oksidasi (pengoksigenan) adalah peristiwa penggabungan suatu zat dengan
oksigen.
Contoh:
Si + O2 → SiO2
4 Fe + 3 O2 → 2
Fe2O3
Reaksi
oksidasi logam dikenal juga dengan nama perkaratan. Reaksi pembakaran juga
termasuk reaksi oksidasi, misalnya pembakaran minyak bumi, kertas, kayu bakar,
dll.
Reaksi
reduksi adalah peristiwa pengeluaran oksigen dari suatu zat.
Contoh:
2 CuO → 2 Cu + O2
H2O → H2 +
O2
2.
Reaksi pelepasan dan pengikatan elektron
Reaksi
oksidasi dan reduksi juga dapat dibedakan dari pelepasan dan penangkapan
elektron.
Oksidasi
adalah peristiwa pelepasan elektron
Contoh:
Na → Na + +
e
Zn → Zn +2 +
2e
Al → Al +3 +
3e
Reduksi
adalah peristiwa penangkapan elektron
Contoh:
Na + + e → Na
Fe +3 + e → Fe +2
Dari
konsep kedua ini dapat disimpulkan bahwa reaksi oksidasi dan reduksi tidak
hanya hanya melibatkan reaksi suatu zat dengan oksigen.
3. Reaksi
penambahan dan pengurangan bilangan oksidasi
Oksidasi
adalah peristiwa naiknya / bertambahnya bilangan oksidasi suatu unsur,
sedangkan reduksi adalah peristiwa turunnya / berkurangnya bilangan oksidasi.
2.9.1 Bilangan oksidasi
Bilangan
oksidasi ( biloks) disebut juga tingkat oksidasi. Bilangan oksidasi diartikan
sebagai muatan yang dimiliki suatu atom dalam keadaan bebas atau dalam senyawa
yang dibentuknya.
Bilangan
oksidasi suatu unsur dapat ditentukan dengan aturan berikut:
1. Biloks
atom dalam unsur adalah nol
Contoh Na, Fe, O2 , H2 memiliki
biloks nol
2. Total
biloks senyawa adalah nol
Contoh H2O, NaOH, CH3COOH, KNO3 total
biloksnya adalah nol
3. Biloks
ion sesuai dengan muatannya
Contoh Na +1 ( = +1), O -2 (
= -2), Fe +3 (= +3)
4. Biloks
unsur golongan I A dalam senyawanya adalah + 1
Contoh Biloks atom Na dalam NaCl adalah + 1
5. Biloks
unsur golongan II A dalam senyawanya adalah + 2
Contoh: Biloks Ca dalam CaCO3 adalah + 2
6. Biloks
unsur golongan VII A dalam senyawa binernya adalah – 1
Contoh: Biloks F dalam senyawa KF dan BaF2 adalah – 1
7. Biloks
unsur oksigen dalam senyawanya adalah – 2
Contoh dalam H2O, Na2O, Al2O3
8. Biloks
unsur hydrogen dalam senyawanya adalah + 1
Contoh dalam H2O, HCl, H2SO4
Catatan
Penting:
Biloks H = -1 dalam senyawa hidrida misal NaH, LiH, CaH2
Biloks O = -1 dalam senyawa peroksida misal H2O2
2.9.2 Oksidator dan reduktor
Oksidator
adalah istilah untuk zat yang mengalami reduksi (biloksnya turun), sedangkan
Reduktor adalah zat yang mengalami reaksi oksidasi (biloksnya
naik/bertambah).
Contoh:
Pada
reaksi 2Na + 2H2O
→ 2NaOH + H2
Reduktor
adalah Na sebab biloksnya naik dari 0 ke +1
Oksidator
adalah H2O sebab biloks H berubah dari +1 ke 0
2.10 CARA MEMBERI NAMA SENYAWA KIMIA
Setiap senyawa
mempunyai nama yang khas. Himpunan
kimia sedunia, IUPAC (International Union of Pure and Applied
Chemistry), telah membuat aturan
mengenai penamaan senyawa kimia. Di dunia, ada beberapa senyawa
yang memiliki dua nama, yaitu satu nama yang sesuai dengn aturan IUPAC, dan
satu nama lagi berasal dari nama trivial atau nama dagang.
Berikut ini adalah beberapa aturan tata nama senyawa sesuai dengan aturan IUPAC
TATA NAMA SENYAWA ANORGANIK
Yang akan di bahas pada tata nama senyawa
anorganik ini antara lain : tata nama
senyawa biner, poliatomik, basa, dan asam. Berikut adalah penjelasannya.
1. Tata nama senyawa biner
Senyawa biner adalah senyawa yang tersusun
atas dua unsur. Kadua unsur itu dapat berupaunsur logam dan unsur nonlogam atau unsur nonlogam dan unsur nonlogam.
Unsur logam dalam senyawa biner biasanya merupakan kation (ion positif) (Baca
juga tentang reaksi
ionisasi dan pembentukan ion disini sedangkan
unsur nonlogam dalam senyawa biner biasanya merupakan anion (ion negatif).
a. Tata nama senyawa biner logam dan
nonlogam
Terdapat tiga aturan untuk penamaan
senyawa yang tersusun atas unsur logam dan unsur nonlogam. Berikut adalah
aturannya :
·
Untuk unsur logam yang hanya mempunyai
satu bilangan oksidasi, penamaannya dengan cara menyebutkan nama unsur nonlogam
didepan dan kemudian nama unsur nonlogam disertai akhiran ida
Nama
unsur logam + nama unsur nonlogam –ida
Contoh
:
1. LiF
= Li (litium) + F (flour) = Litium Flourida
2. MgCl2
= Mg (magnesium) + Cl(klor) = Magnesium Klorida
3. BeO
= Be (berrilium) + O (oksigen) = Berrilium Oksida
4. K2S
= K (Kalium) + S (sulfur) = Kalium Sulfida
5. Al2O3
= Al (alumunium) + O (oksigen) = Alumunium Oksida
6. MgBr2
= Mg (magnesium) + Br (bromium) = Magnesium Bromida
·
Untuk unsur logam yang mempunyai lebih
dari satu bilangan oksidasi, penamaan adalah dengan cara menuliskan nama unsur
logam disertai dengan menuliskan bilangan oksidasinya dengan menggunakan angka
romawi di dalam tanda kurung dan nama nonlogam di belakang disertai akhiran
–ida. Untuk penamaan dengan metode ini dapat dengan menggunakan nama lokal atau
nama dagang untuk nama unsur logamnya.
Nama
unsur nonlogam (bilangan oksidasi dalam angka romawi) + nama unsur nonlogam
–ida
Contoh :
1. CuCI
= Tembaga (I) Klorida
2. SnO
= Timah (II) Oksida
3. CuCI2
= Tembaga (II) Klorida
4. SnO2
= Timah (IV) Oksida
5. PbO
= Timbel (II) Oksida
6. CuI2
= Tembaga (II) Iodida
7. MnO2
= Mangan (IV) Oksida
8. AgF
= Perak (I) Flourida
9. HgO
= Mercuri (II) Oksida
10. PbCl2
= Timbel (II) Klorida
11. Fe2O3
= Besi (III) Oksida
12. SnF2
= Timah (II) Flourida
13. AuCl3
= Emas (III) Klorida
·
Untuk unsur logam yang mempunyai lebih
dari satu bilangan oksidasi, ada dua cara :
1. Jika
bilangan oksidasi pada unsur logam lebih kecil, maka diakhiri dengan –o
2. Jika
bilangan oksidasi pada unsur logam lebih besar, maka diakhiri dengan –i
Nama
unsur logam –i atau –o + nama unsur nonlogam
Cara mengetahui apakah bilangan oksidasi
suatu unsur lebih besar atau lebih kecil adalah dengan melihat SPU (Sistem
Periodik Unsur). Lihatlah tepat diatas lambing unsur, angka tersebut merupakan
angka yang menunjukkan bilangan oksidasi suatu unsur. Misal unsur H hanya
mempunyai satu bilangan oksidasi, yaitu +1, sementara unsur Fe mempunyai dua
bilangan oksidasi, yaitu +2, dan +3 (artinya bilangan oksidasi +2 merupakan
bilangan oksidasi kecil dari unsur Fe, dan bilangan oksidasi +3 merupakan
bilangan oksidasi besar dari unsur Fe).
Contoh :
1. PbO
= Plumbo Oksida (bilangan oksidasi Pb = +2 => lebih kecil)
2. CuCI2
= Cupri Iodida (bilangan oksidasi Cu = +2 => lebih besar)
3. CuCl
= Cupro Klorida (bilangan oksidasi Cu = +1 => lebih kecil)
4. CuCl2
= Cupri Klorida (bilangan oksidasi Cu = +2 => lebih besar)
5. FeCI2
= Ferro Klorida (bilangan oksidasi Fe = +2 => lebih kecil)
6. FeCl3
= Ferri Klorida (bilangan oksidasi Fe = +3 => lebih besar)
7. HgO
= Hidra Argiri Oksida (bilangan oksidasi Hg = +2 => lebih besar)
8. FeO3
= Ferri Oksida (bilangan oksidasi Fe = +3 => lebih besar)
9. SnF2
= Stanno Flourida (bilangan oksidasi Sn = +2 => lebih kecil)
10. AuCl3
= Auri Klorida (bilangan oksidasi Fe = +3 => lebih besar)
b. Tata nama senyawa biner nonlogam dan nonlogam
·
Unsur dengan atom yang cenderung
bermuatan positif, diletakkan didepan. Sementara unsur dengan atom yang
cenderung bermuatan negatif diletakkan dibelakang. Adapun urutannya adalah B –
Si – C – Sb – As – P – N – H – Te – Se – S – I – Br – CI – O – F
Contoh :
1. Amonia
= NH3 bukan H3N
2. Air
= H2O bukan OH2
·
Penulisan senyawa nonlogam dan nonlogam
adalah, dengan menuliskan nama unsur nonlogam diawali dengan awalan yang
menunjukkan jumlah unsur nonlogam dan nama unsur nonlogam diawali dengan awalan
yang menunjukan jumlah unsur nonlogam serta diikuti dengan akhiran –ida. Awalan
pada yang menunjukan jumlah unsur nonlogam ditulis dengan bahasa yunani. Untuk
awalan yang menunjukkan jumlah satu pada unsur nonlogam yang didepan tidak
perlu ditulis (awalan yang menunjukkan jumlah unsur nonlogam) - nama unsur
nonlogam + (awalan yang menunjukkan jumlah unsur nonlogam) – nama unsur
nonlogam –ida
Jumlah unsur yang menunjukkan jumlah unsur
dalam bahasa yunani
§
Satu = mono
§
Dua = di
§
Tiga = tri
§
Empat = tetra
§
Lima = penta
§
Enam = heksa
§
Tujuh = hepta
§
Delapan = okta
§
Sembilan = nona
§
Sepuluh = deka
Contoh :
1. PCl3
= Fosfor Triklorida (indeks 1 pada unsur P tidak perlu ditulis)
2. N2O3
= Dinitrogen Trioksida
3. NO
= Nitrogen Oksida
4. CCI4
= Karbon Tetraklorida
5. NO2
= Nitrogen Dioksida
6. SO2
= Sulfur Dioksida
7. SO3
= Sulfur Trioksida
8. N2O5
= Dinitrogen Pentaoksida
9. CI2O7
= Dikloro Heptaoksida
10. CO2
= Karbon Dioksida
TATA NAMA SENYAWA ASAM
Asam
merupakan zat yang menghasilkan ion hIdrogen (H+) jika dilarutkan ke dalam air.
Untuk senyawa asam biner,
tata namanya diawali dengan kata asam dan diikuti dengan nama unsur yang
mengikutinya. Sedangkan untuk senyawa
asam poliatomik, penamaannya diawali dengan kata asam dan diikuti
dengan sisanya, yaitu anion.


Asam
+ sisanya
Contoh :
1. HBr
= Asam Bromida
2. H2CO3
= Asam Karbonat
3. H2SO4
= Asam Sulfat
4. H2SO3
= Asam Sulfit
5. H3PO4
= Asam Fosfat
6. H3PO3
= Asam Fosfit
7. HNO2
= Asam Nitrit
8. HNO3
= Asam Nitrat
9. H2C2O4
= Asam Aksalat
10. CH3COOH
= Asam Asetat
TATA NAMA SENYAWA BASA
Basa
merupakan zat yang menghasilkan ion hidroksida (OH-) jika dilarutkan di dalam
air. Tata nama senyawa logam adalah tata nama unsur
logam dan diikuti –hidroksida.
Tata
nama logam + hidroksida
Contoh :
1. Al(OH)3
= Alumunium Hidroksida
2. Ba(OH)2
= Barium Hidroksida
3. Cu(OH)2
= Tembaga (II) Hidroksida atau Cupri Hidroksida (bilangan oksidasi CU = +2,
lebih besar)
4. Fe(OH)3
= Besi (III) Hidroksida atau Ferri Hidroksida (bilangan oksidasi Fe = +3. Lebih
besar)
5. AgOH
= Perak Hidroksida
6. Au(OH)2
= Emas (II) Hidroksida atau Aurri Hidroksida (bilangan oksidasi Au = +2, lebih
besar)
7. Be(OH)2
= Berrilium Hidroksida
8. Pb(OH)4
= Timbal (IV) atau Plumbi Hidroksida (bilangan oksidasi Pb = +4, lebih besar)
TATA NAMA SENYAWA POLIATOMIK
Untuk senyawa poliatomik ini, anda harus
bisa menerapkan tata nama senyawa biner, baik logam dan nonlogam maupun
nonlogam dan nonlogam, serta tabel kation dan anion. Untuk senyawa poliatomik
yang tersusun atas kation dan anion poliatomik, susunannya adalah kation
diikuti dengan nama anion.
Contoh :
1. MgCO3
= Magnesium Karbonat
2. KClO3
= Kalium Klorat
3. Fe(NO3)3
= Besi (III) Nitrat atau Ferri Nitrat (Perhatikan unsur logam dan kationnya).
DAFTAR PUSTAKA
http://sapakabar.blogspot.co.id/2015/02/tata-nama-senyawa-kimia-sederhana.html